Cho 12 gam hỗn hợp hai kim loại thuộc nhóm IA và ở hai chu kì liên tiếp trong bảng tuần hoàn, tác dụng với nước dư thu được 4,48 lít khí Hidro (đktc). Xác định tên của hai kim loại đem dùng
Cho 10,2 gam hỗn hợp hai kim loại thuộc nhóm IA và ở hai chu kì liên tiếp trong bảng tuần hoàn, tác dụng với H2O dư thu được 5,6 lít khí H2 (đktc). Xác định tên của hai kim loại đem dùng
A. Li, Na
B. Na, K
C. Li, Be
D. Li, K
Đáp án A
Gọi kim loại thuộc hai chu kì liên tiếp và thuộc nhóm IA là: X và Y (MX < MY)
Gọi kim loại chung của hai kim loại này là ![]()
2![]() + 2H2O --> 2
+ 2H2O --> 2![]() OH + H2
OH + H2![]() (1)
(1)
(mol) 0,5 ![]() 0,25
0,25
Ta có: nH2 = 5,6/22,4 = 0,25 (mol). Từ (1) => nA = 0,5(mol)
=> MA = 10,2/0,5= 20, 4 => MX < MA = 20, 4 < MY
Vậy X là Li (M = 7) và Y là Na ( M=23)
Cho 8,8 gam một hỗn hợp hai kim loại nằm ở hai chu kì liên tiếp nhau và thuộc nhóm IIIA, tác dụng với HCl dư thì thu được 6,72 lít khí hidro (đktc). Dựa vào bảng tuần hoàn cho biết tên hai kim loại đó
A. B và Al
B. Al và Ga
C. Ga và In
D. In và Ti
Đáp án B
Hướng dẫn Đặt CT chung của 2 kim loại nhóm IIIA là M, nguyên tử khối trung bình là ![]()
Phương trình hóa học có dạng: 2M + 6HCl → 2MCl3 + 3H2
![]()
theo đầu bài : ![]() .0,2 = 8,8 →
.0,2 = 8,8 → ![]() = 44
= 44
2 kim loại thuộc hai chu kì liên tiếp của nhóm IIIA, một kim loại có nguyên tử khối nhỏ hơn 44 và một kim loại có nguyên tử khối lơn hơn 44
2 KL là: Al (M = 27 < 44) và Ga (M = 69,72 > 44)
Cho 24,95 gam một hỗn hợp hai kim loại nằm ở hai chu kì liên tiếp và đều thuộc nhóm IIA của bảng tuần hoàn tác dụng với axit H2SO4 loãng thu được 4,48 lít khí H2 (đktc). Hai kim loại đó là
A. Ca và Sr
B. Sr và Ba
C. Be và Ca
D. Ca và Ba
Đáp án B
Gọi công thức chung của hai kim loại thuộc nhóm IIA là M .
Có phản ứng:
![]()
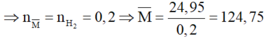
Do đó hỗn hợp cần có 1 kim loại có M < 124,75 và 1 kim loại có khối lượng mol lớn hơn 124,75.
Mà hai kim loại trong hỗn hợp ở hai chu kì liên tiếp và thuộc nhóm IIA.
Nên hai kim loại đó là Se và Ba.
Chú ý: Khi cho hỗn hợp hai kim loại có cùng hóa trị thì ta thường sử dụng công thức trung bình của hai kim loại.
Cho 24,95 gam một hỗn hợp hai kim loại nằm ở hai chu kì liên tiếp và đều thuộc nhóm IIA của bảng tuần hoàn tác dụng với axit H2SO4 loãng thu được 4,48 lít khí H2 (đktc). Hai kim loại đó là:
A. Ca và Sr
B. Sr và Ba
C. Be và Ca
D. Ca và Ba
Đáp án B
Gọi công thức chung của hai kim loại thuộc nhóm IIA là M
Có phản ứng:
![]()
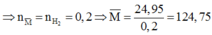
Do đó hỗn hợp cần có 1 kim loại có M < 124,75 và 1 kim loại có khối lượng mol lớn hơn 124,75.
Mà hai kim loại trong hỗn hợp ở hai chu kì liên tiếp và thuộc nhóm IIA.
Nên hai kim loại đó là Se và Ba.
Chú ý: Khi cho hỗn hợp hai kim loại có cùng hóa trị thì ta thường sử dụng công thức trung bình của hai kim loại.
Câu 32 (0,5 điểm): Cho 33,15 gam hỗn hợp A gồm hai muối cacbonat của hai kim loại nhóm IA, hai chu kì kế tiếp nhau trong bảng tuần hoàn tác dụng hết với dung dịch HCl dư thu được 4,48 lít khí (đktc). Tìm công thức hai muối trong hỗn hợp A và tính khối lượng muối clorua thu được sau phản ứng.
Cho 15,5g hỗn hợp gồm hai kim loại liên tiếp ở hai chu kì kế tiếp nhau
trong bảng tuần hoàn tác dụng hết với nước thu được 5,6 lít khí H2 (đktc) và dung
dịch kiềm
a. Xác định tên hai kim loại đó và tính phần trăm khối lượng mỗi kim loại?
b. Tính thể tích dung dịch HCl 1,5M cần dùng để trung hòa dung dịch kiềm và
khối lượng muối clorua thu được?
Hỗn hợp X gồm 2 kim loại thuộc hai chu kì liên tiếp nhau và thuộc nhóm IA. Cho 5,4 gam X tác dụng với dung dịch H2SO4 loãng (dư) thì thu được 2,24 lít khí hiđro (đktc) và dung dịch B. a. Xác định hai kim loại và % khối lượng mỗi kim loại trong hỗn hợp? b. Tính khối lượng muối thu được khi cô cạn dung dịch B?
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(2X+H_2SO_4\rightarrow X_2SO_4+H_2\)
0,2 \(\leftarrow\) 0,1
\(\Rightarrow\overline{M_X}=\dfrac{5,4}{0,2}=27\) \(\Rightarrow X_1< 27< X_2\)
Mà X1, X2 thuộc nhóm IA
\(\Rightarrow\left\{{}\begin{matrix}X_1:Na\\X_2:K\end{matrix}\right.\) Gọi \(n_{Na}=x\left(mol\right)\) , \(n_K=y\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}BTKL:23x+39y=5,4\\BTe:x+y=2n_{H_2}=0,2\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}x=0,15mol\\y=0,05mol\end{matrix}\right.\)
\(\%m_{Na}=\dfrac{0,15\cdot23}{5,4}\cdot100\%=63,89\%\)
\(\%m_K=100\%-63,89\%=36,11\%\)
Khi cô cạn dung dịch thu được muối: \(\left\{{}\begin{matrix}n_{Na^+}=0,15mol\\n_{K^+}=0,05mol\\n_{SO_4^{2-}}=n_{H_2SO_4}=n_{H_2}=0,1mol\end{matrix}\right.\)
\(\Rightarrow m_{m'}=0,15\cdot23+0,05\cdot39+0,1\cdot\left(32+4\cdot16\right)=15g\)
Cho 7,2 gam hỗn hợp hai kim loại nhóm IA, thuộc hai chu kỳ liên tiếp, tác dụng hết với dung dịch HCl dư thu được 4,48 lít khí hiđro (đktc). Hai kim loại đó là
Gọi CTTQ hai kim loại kiềm là R
$n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
$2R + 2HCl \to 2RCl + H_2$
$n_R = 2n_{H_2} = 0,2.2 = 0,4(mol)$
$\Rightarrow M_R = \dfrac{7,2}{0,4} = 18(g/mol)$
Ta thấy : $M_{Liti} = 7 < 18 < M_{Natri} = 23$
Do đó hai kim loại đó là Liti và Natri
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ \text{Đ}\text{ặt}-chung-2kl:A\\ A+HCl\rightarrow ACl+\dfrac{1}{2}H_2\\ n_A=2.0,2=0,4\left(mol\right)\\ M_A=\dfrac{7,2}{0,4}=18\left(\dfrac{g}{mol}\right)\\ \Rightarrow2KL:Liti\left(Li\right),Natri\left(Na\right)\)
hỗn hợp A gồm 2 kim loại thuộc hai chu kì liên tiếp nhau và thuộc nhóm IA. Cho 5,4 gam A tác dụng với dung dịch H2SO4 1M (dư) thì thu được 2,479 lít khí hidro (đkc) và dung dịch B.
a. xác định kim loại đó
b. tính phần trăm khối lượng mỗi kim loại trong hỗn hợp
c. tính nồng độ mol các chất lượng trong B. Biết lượng H2SO4 dư với lượng phản ứng là 20%
a, \(n_{H_2}=\dfrac{2,479}{24,79}=0,1\left(mol\right)\)
BT e, có: nR = 2nH2 = 0,2 (mol)
\(\Rightarrow\overline{M}_R=\dfrac{5,4}{0,2}=27\left(g/mol\right)\)
Mà: 2 KL thuộc 2 chu kì liên tiếp và thuộc nhóm IA.
→ Na và K.
b, Có: 23nNa + 39nK = 5,4 (1)
BT e, có: nNa + nK = 2nH2 = 0,2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Na}=0,15\left(mol\right)\\n_K=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Na}=\dfrac{0,15.23}{5,4}.100\%\approx63,89\%\\\%m_K\approx36,11\%\end{matrix}\right.\)
b, BTNT H, có: \(n_{H_2SO_4\left(pư\right)}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=0,1.20\%=0,02\left(mol\right)\)
\(\Rightarrow V_{ddH_2SO_4}=\dfrac{0,1+0,02}{1}=0,12\left(l\right)\)
BTNT Na, có: nNa2SO4 = 1/2.nNa = 0,075 (mol)
BTNT K, có: nK2SO4 = 1/2.nK = 0,025 (mol)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0,02}{0,12}=\dfrac{1}{6}\left(M\right)\\C_{M_{Na_2SO_4}}=\dfrac{0,075}{0,12}=0,625\left(M\right)\\C_{M_{K_2SO_4}}=\dfrac{0,025}{0,12}=\dfrac{5}{24}\left(M\right)\end{matrix}\right.\)